tendencja do przyjmowania dodatkowego elektronu przez atomy fluorowców
Arkusz z chemii rozszerzonej maj 2021
Wróć do listyAtomy fluorowców wykazują wyraźną tendencję do przyjęcia dodatkowego elektronu i przejścia w jon X⁻ lub też – gdy różnica elektroujemności fluorowca i łączącego się z nim pierwiastka jest mała – do utworzenia wiązania kowalencyjnego. W szczególnych warunkach może nastąpić oderwanie elektronu od obojętnego atomu fluorowca i utworzenie jonu X⁺ .
1. Uzupełnij poniższy schemat tak, aby przedstawiał on graficzny zapis konfiguracji elektronowej kationu bromoniowego Br+ (stan podstawowy). W tym zapisie uwzględnij numery powłok i symbole podpowłok.
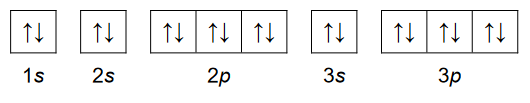
2. Spośród wymienionych poniżej substancji wybierz te, w skład których wchodzą jony Cl⁻ . Podkreśl wzory wybranych związków.
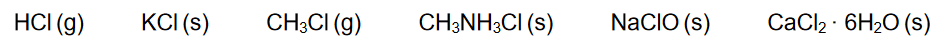
3. Poniżej przedstawiono schematy czterech przemian chemicznych A, B, C i D, w których jednym z substratów jest chlor.
A. metan →⎯chlorometan
B. eten → 1,2-dichloroetan
C. benzen →⎯chlorobenzen
D. toluen (metylobenzen) → chlorofenylometan (C6H5CH2 Cl)
3.1 Spośród przemian oznaczonych literami A, B, C i D wybierz te, w przebiegu których udział biorą rodniki chloru. Napisz litery, którymi oznaczono te przemiany.
3.2 W reakcjach substytucji elektrofilowej i addycji elektrofilowej bierze udział tzw. elektrofil, czyli jon lub cząsteczka z niedomiarem elektronów. Substytucja elektrofilowa w pierścieniu aromatycznym przebiega przez kilka etapów. Najpierw powstaje nietrwałe połączenie (kompleks 𝜋), które następnie przekształca się w karbokation, tzw. kompleks 𝜎, co wiąże się z deformacją układu wiązań i utratą charakteru aromatycznego. Po odłączeniu protonu układ wiązań odzyskuje charakter aromatyczny. Opisane etapy zilustrowano na poniższym schemacie.
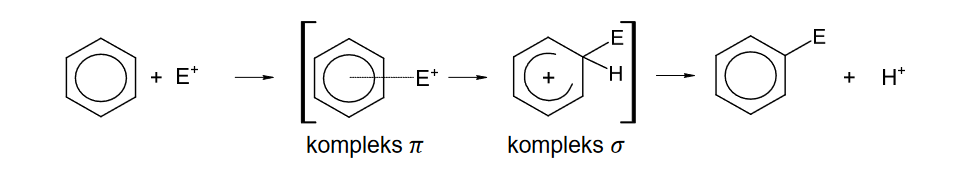
Szybkość tworzenia produktu substytucji elektrofilowej zależy od szybkości, z jaką powstaje kompleks 𝜎.
Reakcje addycji elektrofilowej przebiegają także poprzez tworzenie kompleksu 𝜋 oraz karbokationu, jednak kończą się połączeniem z czynnikiem nukleofilowym, utworzonym w trakcie przemiany.
Uzupełnij poniższe zdania. Wybierz i podkreśl jedną odpowiedź spośród podanych w każdym nawiasie.
Przykładem reakcji addycji elektrofilowej jest przemiana oznaczona literą (A / B / C / D). W reakcji addycji cząsteczka chloru ulega rozpadowi na kation chloroniowy i anion chlorkowy
– wskutek oddziaływania z elektronami wiązania podwójnego. W wyniku działania czynnika elektrofilowego na podwójne wiązanie węglowodoru powstaje, jako produkt przejściowy, organiczny (kation / rodnik), następnie przyłączający jon (Cl⁺ / Cl⁻).
Przykładem reakcji substytucji elektrofilowej jest przemiana oznaczona literą (A / B / C / D). W tej przemianie uczestniczy katalizator, który przez utworzenie jonu kompleksowego powoduje rozpad cząsteczki chloru i wytworzenie czynnika elektrofilowego. Tym katalizatorem jest (FeCl3 / H2SO4). W opisanej przemianie najwolniejszym etapem jest ten, w którym (tworzy się kompleks 𝜎 / następuje eliminacja protonu).

KOREPETYCJE