Zadanie 14.
2015 maj sr
Wróć do listyKwas szczawiowy (etanodiowy) to najprostszy kwas dikarboksylowy o wzorze sumarycznym
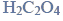
Szczawian magnezu
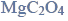
jest bezbarwnym krystalicznym ciałem stałym, które trudno rozpuszcza się w wodzie. Kationy magnezu mają zdolność tworzenia z anionami szczawianowymi jonów kompleksowych o wzorze
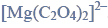
Sole zawierające ten jon są rozpuszczalne w wodzie.
W poniższej tabeli przedstawiono informacje o rozpuszczalności w wodzie szczawianów wybranych metali w temperaturze pokojowej.

Na podstawie: J. Minczewski, Z. Marczenko, Chemia analityczna. Podstawy teoretyczne i analiza jakościowa, Warszawa 2001 oraz W. Mizerski, Tablice chemiczne, Warszawa 1997.
1. Sformułuj hipotezę na temat zachowania szczawianu magnezu w kontakcie z roztworem zawierającym jony szczawianowe. Uwzględnij wytrącanie lub roztwarzanie związków magnezu.
2. Zaprojektuj doświadczenie, którego przebieg potwierdzi sformułowaną hipotezę. Uzupełnij poniższy schemat − wpisz wzory soli wybranych spośród następujących:
− CaC2O4
− K2C2O4
− MgCl2
− MgCO3
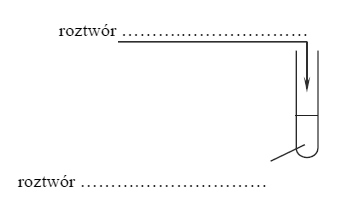
3. Napisz w formie jonowej skróconej równania reakcji zachodzących w czasie doświadczenia.
KOREPETYCJE