Oblicz stężenie molowe jonów ołowiu(II) w roztworze…
Arkusz maturalny z chemii rozszerzonej czerwiec 2019 nowa formuła
Wróć do listyIloczyn rozpuszczalności Ks soli i wodorotlenków jest stałą równowagi dynamicznej, jaka ustala się między nierozpuszczoną substancją a jej roztworem nasyconym.
Chlorek ołowiu(II) jest związkiem trudno rozpuszczalnym w wodzie. Iloczyn rozpuszczalności tej soli wyraża się równaniem
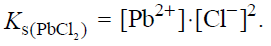
W temperaturze 298 K jego wartość jest równa
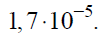
Jeżeli stężenie jednego z jonów w roztworze się zmieni, np. przez rozpuszczenie innej
substancji, która jest mocnym elektrolitem i dysocjuje z wytworzeniem takich jonów, zmienia się stężenie drugiego jonu, tak aby – zgodnie z regułą przekory – zachowana była stała wartość iloczynu rozpuszczalności.
Na podstawie: K.-H. Lautenschläger, W. Schröter, A. Wanninger, Nowoczesne kompendium chemii, Warszawa 2007.
Przygotowano 100 cm3 nasyconego wodnego roztworu chlorku ołowiu(II) o temperaturze
298 K. Do przygotowanego roztworu dodano 100 cm3 wodnego roztworu chlorku sodu
o stężeniu 1,0 mol⋅dm−3.
Oblicz stężenie molowe jonów ołowiu(II) w roztworze otrzymanym w opisany powyżej sposób w temperaturze 298 K. W obliczeniach pomiń stężenie jonów chlorkowych pochodzących od trudno rozpuszczalnej soli.
KOREPETYCJE