Obliczanie stałej stężeniowej reakcji.
Arkusz maturalny z chemii rozszerzonej czerwiec 2017 stara formuła
Wróć do listyW zamkniętym naczyniu pomiędzy substancjami X, Y oraz Z, które w temperaturze T i pod ciśnieniem p są gazami, ustala się stan równowagi chemicznej.
Zmianę liczby moli reagentów X, Y oraz Z w trakcie procesu przedstawia poniższy wykres.
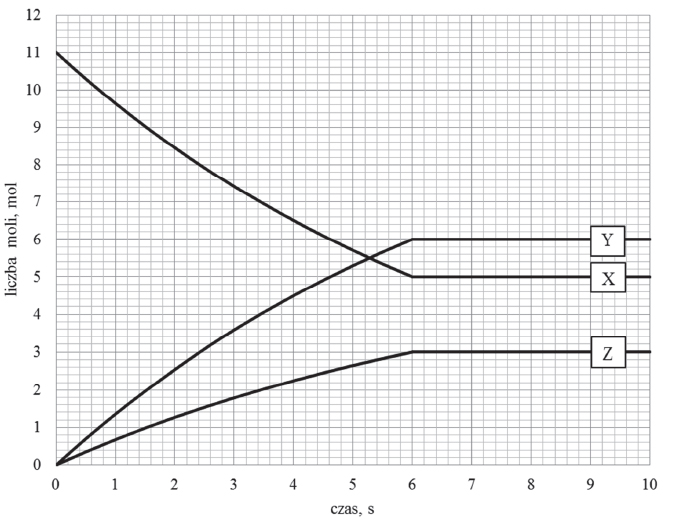
Reakcja, dla której zmianę liczby moli reagentów przedstawiono na wykresie, przebiegała w reaktorze o pojemności 4 dm3. W temperaturze T i pod ciśnieniem p do reaktora wprowadzono substrat reakcji X i badano zmiany liczby moli reagentów w trakcie trwania procesu prowadzącego do ustalenia stanu równowagi dynamicznej.
Oblicz stężeniową stałą równowagi Kc opisanego procesu w temperaturze T.
KOREPETYCJE