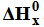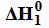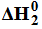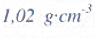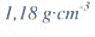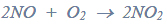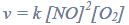Miareczkowanie. Wykres miareczkowania.
Arkusz maturalny z chemii rozszerzonej maj 2008
Do 100 cm3 wodnego roztworu wodorotlenku sodu dodawano kroplami kwas solny o stężeniu 0,20 mol/dm3 i za pomocą pehametru mierzono pH mieszaniny reakcyjnej. Otrzymane wyniki umieszczono na wykresie ilustrującym zależność pH od objętości dodanego HCl.
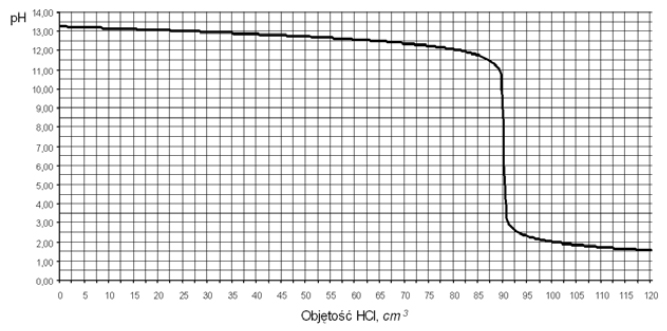
a) Z powyższego wykresu odczytaj objętość kwasu solnego potrzebną do zobojętnienia wodorotlenku sodu znajdującego się w badanym roztworze. b) Oblicz stężenie molowe badanego roztworu wodorotlenku sodu. Wynik podaj z dokładnością do dwóch miejsc po przecinku.
Elektroliza wody.
Arkusz maturalny z chemii rozszerzonej maj 2008
Chemicznie czysta woda nie ulega elektrolizie. Aby umożliwić ten proces, należy w wodzie rozpuścić odpowiednią substancję. Zachodzi wtedy elektrolityczny rozkład wody, którego przebieg ilustruje następujące równanie:

Oblicz, jaką objętość, w temperaturze 22°C i pod ciśnieniem 1000 hPa, zajmie tlen otrzymany w wyniku elektrolitycznego rozkładu 100 gramów wody. Wartość stałej gazowej R wynosi
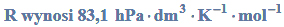
Zadanie 4.
2007 czerwiec
Oblicz masę 4 dm3 CO2 w temperaturze 300 K i pod ciśnieniem 1500 hPa. Stała gazowa