Dimetyloglioksym jest związkiem organicznym o następującym wzorze:
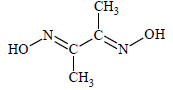
Związek ten jest wykorzystywany w analizie chemicznej między innymi do wykrywania i określania ilości jonów niklu(II), z którymi tworzy trudno rozpuszczalny w wodzie osad dimetyloglioksymianu niklu(II) o różowym zabarwieniu. Reakcja ta przebiega zgodnie z równaniem
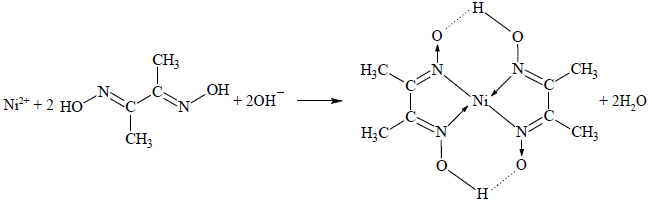
Na podst.: J. Minczewski, Z. Marczenko, Chemia analityczna 2. Chemiczne metody analizy ilościowej, Warszawa 1998, s. 179–181.
Aby wyznaczyć masę niklu w postaci jonów Ni2+ w próbce pewnego roztworu o objętości 100,00 cm3, z próbki tej pobrano trzy równe porcje oznaczone numerami I–III o objętości 10,00 cm3 każda. Pobranie do analizy trzech, a nie jednej porcji badanego roztworu miało na celu zmniejszenie wpływu na wynik analizy błędów przypadkowych. Każdą porcję poddano niezależnie takim samym czynnościom laboratoryjnym, uzyskując wyniki, z których obliczono średnią arytmetyczną. Pobrane porcje wprowadzono do oddzielnych zlewek, zakwaszono, uzupełniono wodą destylowaną do objętości 50 cm3 i ogrzano do temperatury ok. 60 ºC. Następnie do każdej zlewki wprowadzono niewielki nadmiar alkoholowego roztworu dimetyloglioksymu i mieszając, dodano wodę amoniakalną w celu osiągnięcia odpowiedniego pH roztworu. We wszystkich naczyniach zaobserwowano wytrącenie różowego osadu. Osad otrzymany w każdej zlewce odsączono pod zmniejszonym ciśnieniem w uprzednio zważonych tyglach szklanych z porowatym dnem, które pełnią podwójną funkcję: sączka i tygla. Odsączone osady przemyto i wysuszono do stałej masy.
W poniższej tabeli zestawiono wyniki pomiarów masy pustych tygli oraz tygli z osadem dla trzech porcji, które pobrano z badanego roztworu. Pomiary masy wykonano na wadze analitycznej z dokładnością do 0,1 mg.
Na podstawie: J. Minczewski, Z. Marczenko, Chemia analityczna 2. Chemiczne metody analizy ilościowej, Warszawa 1998, s. 179–181; T. Lipiec, Z.S. Szmal, Chemia analityczna z elementami analizy instrumentalnej, Warszawa 1976, s. 330
a) Uzupełnij tabelę, wpisując masę osadów dla trzech porcji badanego roztworu oraz średnią masę osadu.

b) Oblicz, ile gramów niklu w postaci jonów Ni2+ zawierała próbka 100,00 cm3 badanego roztworu, wykorzystując średnią masę osadu dimetyloglioksymianu niklu(II). Masa molowa dimetyloglioksymianu niklu(II) jest równa
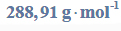
Błąd bezwzględny, jakim jest obarczony wynik analizy dla danej porcji, jest różnicą\ między tym wynikiem a wartością rzeczywistą, której nie znamy. Przyjmujemy, że odpowiada jej obliczona średnia arytmetyczna:
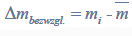
gdzie i oznacza numer porcji.
Błąd względny jest stosunkiem błędu bezwzględnego do wartości rzeczywistej wyrażonym w procentach. W tym przypadku nieznaną wartość rzeczywistą również zastępujemy średnią arytmetyczną:
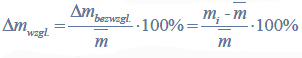
c) Wskaż porcję (I, II albo III), dla której wynik analizy najbardziej odbiega od średniej masy niklu i oblicz błąd względny wyznaczenia masy niklu w postaci jonów Ni2+ w badanym roztworze opisaną metodą dla tej porcji.