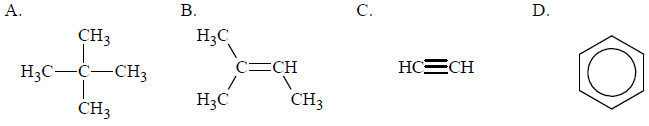
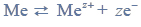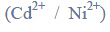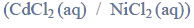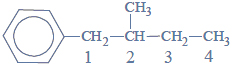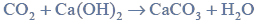Ciąg przemian.
Arkusz maturalny z chemii rozszerzonej maj 2016 stara formuła
Przeprowadzono ciąg przemian opisany poniższym schematem.
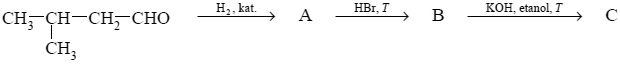
Napisz równanie reakcji prowadzącej do otrzymania produktu A. Zastosuj wzory półstrukturalne (grupowe) związków organicznych.
Reakcje charakterystyczne aldehydów.
Arkusz maturalny z chemii rozszerzonej maj 2016 stara formuła
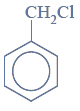
Przeprowadzono ciąg przemian opisany poniższym schematem.
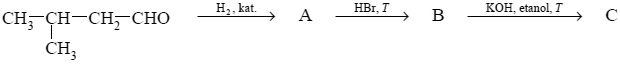
Uzupełnij poniższą tabelę. Podaj wzór półstrukturalny (grupowy) związku organicznego oznaczonego na schemacie literą B. Określ typ reakcji (addycja, eliminacja, substytucja), w wyniku której powstaje związek C.
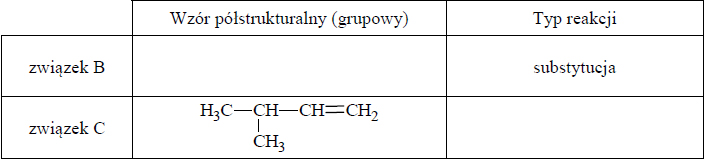
Wzór aldehydu cynamonowego.
Arkusz maturalny z chemii rozszerzonej maj 2016 stara formuła
Aldehyd cynamonowy to związek o wzorze:
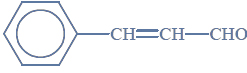
Aldehyd ten występuje w przyrodzie w konfiguracji trans.
Napisz wzór izomeru trans aldehydu cynamonowego.
Aldehyd cynamonowy.
Arkusz maturalny z chemii rozszerzonej maj 2016 stara formuła
Aldehyd cynamonowy to związek o wzorze:

Aldehyd ten występuje w przyrodzie w konfiguracji trans.
Oceń, czy poniższe informacje są prawdziwe.
Zaznacz P, jeśli informacja jest prawdziwa, albo F – jeżeli jest fałszywa.