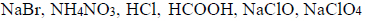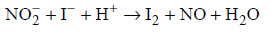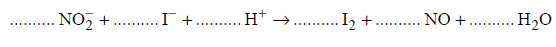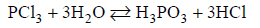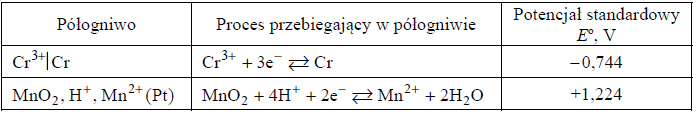Rozpoznawanie pierwiastka na podstawie konfiguracji elektronów walencyjnych.
Arkusz maturalny z chemii rozszerzonej maj 2017 stara formuła
Dwa pierwiastki umownie oznaczone literami X i Z leżą w czwartym okresie układu okresowego pierwiastków. Ponadto wiadomo, że w stanie podstawowym:
– atom pierwiastka X ma na ostatniej powłoce sześć elektronów;
– atom pierwiastka Z ma łącznie na ostatniej powłoce i na podpowłoce 3d sześć elektronów.
1. Uzupełnij poniższą tabelę. Wpisz symbole pierwiastków X i Z, dane dotyczące ich położenia w układzie okresowym oraz symbol bloku konfiguracyjnego, do którego należy każdy z pierwiastków.

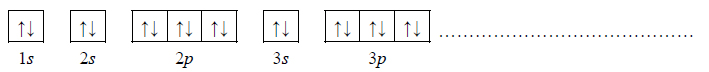
2. Wybierz ten pierwiastek (X albo Z), którego atomy w stanie podstawowym mają większą liczbę elektronów niesparowanych. Uzupełnij poniższy zapis, tak aby przedstawiał on konfigurację elektronową atomu w stanie podstawowym wybranego pierwiastka. Zastosuj schematy klatkowe, podaj numery powłok i symbole podpowłok.
3. Napisz wzór sumaryczny wodorku pierwiastka X oraz wzór sumaryczny tlenku pierwiastka Z, w którym ten pierwiastek przyjmuje maksymalny stopień utlenienia.
Przemiany promieniotwórcze izotopu radu 226
Arkusz maturalny z chemii rozszerzonej maj 2017 stara formuła
Izotop radu 226Ra ulega rozpadowi α. Tej przemianie towarzyszy emisja promieniowania γ. Cząstki α emitowane przez rad mogą służyć do wybijania neutronów z lekkich jąder, np. berylu 9Be.
Na podstawie: A. Czerwiński, Energia jądrowa i promieniotwórczość, Warszawa 1998.
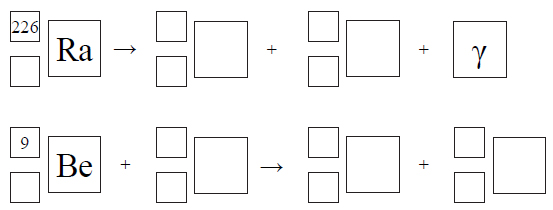
Napisz równania opisanych przemian jądrowych. Uzupełnij wszystkie pola w poniższych schematach.
Rozkład promieniotwórczy izotopu polonu 216
Arkusz maturalny z chemii rozszerzonej maj 2017 stara formuła
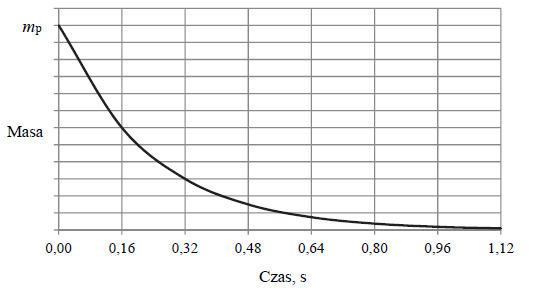
Poniżej przedstawiono wykres zależności masy promieniotwórczego izotopu polonu 216Po od czasu. Symbol mp oznacza początkową masę izotopu.
Na podstawie: A. Czerwiński, Energia jądrowa i promieniotwórczość, Warszawa 1998.
Odczytaj z wykresu wartość okresu półtrwania izotopu polonu 216Po . Określ, po ilu sekundach w próbce zawierającej 100 mg izotopu polonu 216Po ulegnie rozpadowi 75 mg tego izotopu.
Izotopy miedzi.
Arkusz maturalny z chemii rozszerzonej maj 2017 stara formuła
Masa atomowa izotopu jest w przybliżeniu równa jego liczbie masowej A. Miedź występuje w przyrodzie w postaci dwóch trwałych izotopów. Skład izotopowy miedzi (w zaokrągleniu do jedności) przedstawiono w poniższej tabeli.
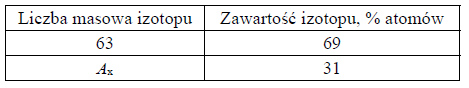
Na podstawie: J. Sawicka, A. Janich-Kilian, W. Cejner-Mania, G. Urbańczyk, Tablice chemiczne, Gdańsk 2001.
Wykonaj obliczenia i podaj liczbę masową Ax drugiego naturalnego izotopu miedzi. Przyjmij, że średnia masa atomowa miedzi jest równa 63,55 u.
Wykrywanie wiązania jonowego w cząsteczkach.
Arkusz maturalny z chemii rozszerzonej maj 2017 stara formuła
Spośród substancji, których wzory podano poniżej, wybierz wszystkie związki jonowe. Podkreśl wzory wybranych substancji.
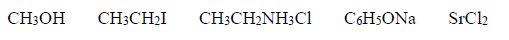
Kształt chloroformu (trichlorometanu) oraz wzór elektronowy.
Arkusz maturalny z chemii rozszerzonej maj 2017 stara formuła
Chloroform (trichlorometan) o wzorze CHCl3 i trichlorek fosforu o wzorze PCl3 są związkami kowalencyjnymi.
1. Określ kształt cząsteczki chloroformu (cząsteczka tetraedryczna, płaska, liniowa).
2. Narysuj wzór elektronowy cząsteczki CHCl3 oraz wzór elektronowy cząsteczki PCl3 – zaznacz kreskami wiązania chemiczne oraz wolne pary elektronowe.
3. Oceń, czy atom centralny w cząsteczce chloroformu i w cząsteczce trichlorku fosforu może tworzyć wiązanie koordynacyjne. Odpowiedź uzasadnij.
Objętość amoniaku w mieszaninie poreakcyjnej.
Arkusz maturalny z chemii rozszerzonej maj 2017 stara formuła
Reakcja syntezy amoniaku przebiega zgodnie z równaniem:
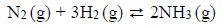
W mieszaninie wodoru i azotu użytej do syntezy amoniaku zawartość wodoru wyrażona w procentach objętościowych jest równa 75%. Wydajność reakcji syntezy amoniaku przeprowadzonej w temperaturze T i pod ciśnieniem p jest równa 93%.
Oblicz wyrażoną w procentach objętościowych zawartość amoniaku w mieszaninie poreakcyjnej.
Arkusz maturalny z chemii rozszerzonej maj 2017 stara formuła
Arkusz maturalny z chemii rozszerzonej maj 2017 stara formuła
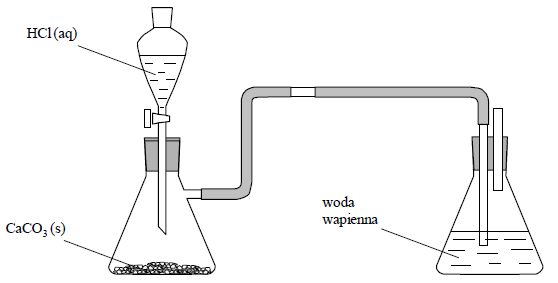
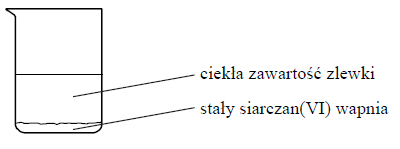
Próbkę czystego węglanu wapnia o masie m prażono przez pewien czas w otwartym naczyniu. Przebiegła wtedy reakcja zilustrowana równaniem:
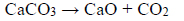
Po przerwaniu ogrzewania stwierdzono, że w naczyniu znajdowała się mieszanina substancji stałych o masie 18,0 gramów. Ustalono, że w tej mieszaninie zawartość węglanu wapnia wyrażona w procentach masowych jest równa 57,5%.
Oblicz masę m próbki węglanu wapnia, którą poddano prażeniu.