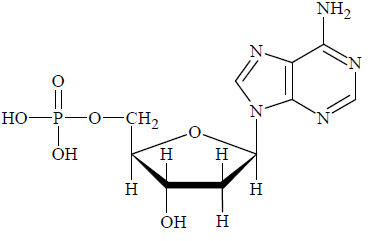
Zadanie 19.
2017 maj SR
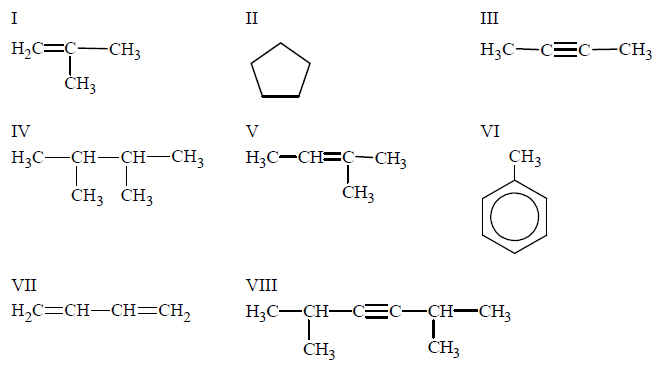
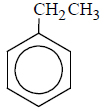
Napisz wzory uproszczone wszystkich pochodnych benzenu, które są izomerami związku o wzorze:
Dlaczego alken B nie występuje w postaci izomerów geometrycznych cis–trans
Arkusz maturalny z chemii rozszerzonej maj 2017 stara formuła
Spośród izomerycznych alkenów o wzorze sumarycznym C6H12 tylko alkeny A i B utworzyły w reakcji z HCl (jako produkt główny) halogenek alkilowy o wzorze:
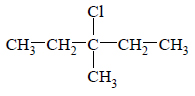
O tych alkenach wiadomo także, że alken A występuje w postaci izomerów geometrycznych cis–trans, a alken B – nie.
Napisz wzory półstrukturalne (grupowe) alkenów A i B. Wyjaśnij, dlaczego alken B nie występuje w postaci izomerów geometrycznych cis–trans.
Hydroliza halogenków alkilowych.
Arkusz maturalny z chemii rozszerzonej maj 2017 stara formuła
Halogenki alkilów ulegają zasadowej hydrolizie.
1. Napisz w formie jonowej, stosując wzory półstrukturalne (grupowe) związków organicznych, równanie hydrolizy zasadowej 2-bromo-2-metylopropanu. Napisz nazwę systematyczną organicznego produktu tej reakcji.
2. Określ mechanizm (elektrofilowy, nukleofilowy, rodnikowy) opisanej reakcji.
Entalpia tworzenia glicerolu.
Arkusz maturalny z chemii rozszerzonej maj 2017 stara formuła
Standardowa molowa entalpia reakcji spalania glicerolu opisanej równaniem:
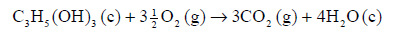
wynosi
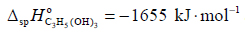
Standardowa entalpia tworzenia wody w ciekłym stanie skupienia
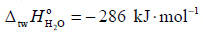
a standardowa entalpia tworzenia gazowego tlenku węgla(IV)
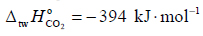
Źródło: J. Sawicka, A. Janich-Kilian, W. Cejner-Mania, G. Urbańczyk, Tablice chemiczne, Gdańsk 2001.
Na podstawie powyższych danych oblicz standardową entalpię tworzenia glicerolu w ciekłym stanie skupienia
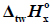
Diasteroizomery kwasu winowego.
Arkusz maturalny z chemii rozszerzonej maj 2017 stara formuła
Poniżej przedstawiono wzór kwasu winowego:
HOOC–CH(OH)–CH(OH)–COOH
1. Przeanalizuj budowę cząsteczki kwasu winowego ze względu na możliwość wystąpienia stereoizomerii i odpowiedz na poniższe pytanie. Wpisz TAK albo NIE do tabeli i podaj uzasadnienie.

2. Uzupełnij poniższe schematy – utwórz wzory w projekcji Fischera dwóch stereoizomerów kwasu winowego będących diastereoizomerami.

Tworzenie wiązania peptydowego.
Arkusz maturalny z chemii rozszerzonej maj 2017 stara formuła
Tripeptyd, którego wzór przedstawiono poniżej, zbudowany jest z reszt trzech różnych aminokwasów.
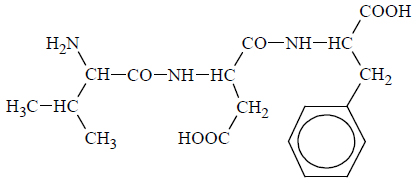
Napisz wzór półstrukturalny (grupowy) tego aminokwasu, którego grupa karboksylowa i grupa aminowa uczestniczyły w utworzeniu wiązania peptydowego w cząsteczce opisanego tripeptydu. Oceń, czy cząsteczka tego aminokwasu jest chiralna. Odpowiedź uzasadnij.
Reakcja polikondensacji, powstawanie nylonu.
Arkusz maturalny z chemii rozszerzonej maj 2017 stara formuła
Nylon jest syntetycznym tworzywem sztucznym o następującym wzorze ogólnym:
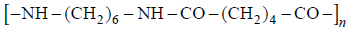
Powstaje on w wyniku reakcji polikondensacji odpowiedniej diaminy i odpowiedniego kwasu dikarboksylowego.
1. Napisz wzory półstrukturalne (grupowe) diaminy oraz kwasu dikarboksylowego, z których to substancji otrzymuje się nylon w reakcji polikondensacji.
2. Poniżej wymieniono nazwy związków, które powstają w wyniku kondensacji związków o mniejszych cząsteczkach.
Spośród wymienionych grup wybierz grupę tych związków, w których cząsteczkach powstały w wyniku reakcji kondensacji takie same wiązania, jakie powstają w wyniku kondensacji diaminy i kwasu dikarboksylowego.
glicerydy, polipeptydy, polisacharydy