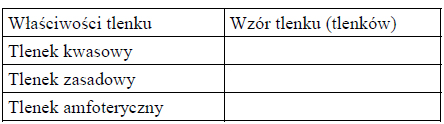
Zadanie 54.
2004 grudzień
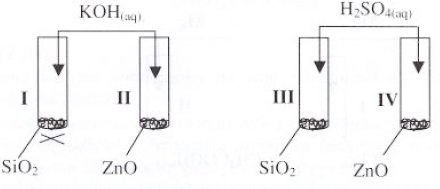
Podaj właściwości chemiczne glinu na przykładzie zachowania wobec tlenu i kwasu solnego.
Diagram fazowy tlenku węgla(IV)
Arkusz maturalny z chemii rozszerzonej maj 2019 nowa formuła
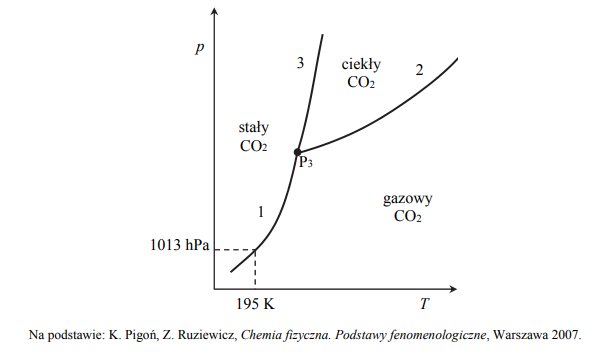
Poniższy diagram fazowy tlenku węgla(IV) przedstawia wartości temperatury i ciśnienia,
w których CO2 występuje w różnych fazach: w stanie stałym, ciekłym lub gazowym. Linie
ciągłe określają warunki temperatury i ciśnienia, w których istnieje trwała równowaga między dwiema fazami. W punkcie oznaczonym symbolem P3 (T = 216 K i p = 5100 hPa) CO2 występuje w trzech fazach znajdujących się w stanie równowagi.
Oceń, czy podane poniżej informacje są prawdziwe. Zaznacz P, jeśli informacja jest prawdziwa, albo F – jeśli jest fałszywa.

W kolbach oznaczonych numerami I, II i III umieszczono w przypadkowej kolejności próbki cynku, magnezu i glinu.
Arkusz maturalny z chemii rozszerzonej maj 2019 nowa formuła
Cynk, magnez i glin w opisanych poniżej doświadczeniach ulegają przemianom zilustrowanym następującymi schematami:
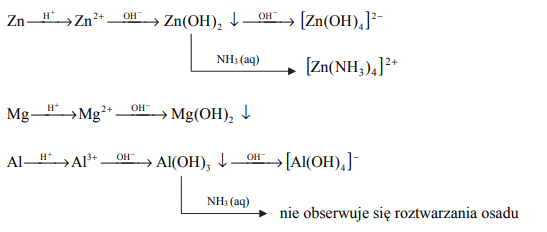
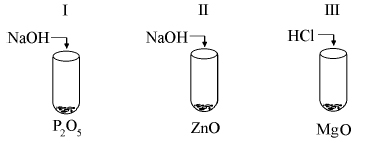
W kolbach oznaczonych numerami I, II i III umieszczono w przypadkowej kolejności próbki cynku, magnezu i glinu. W każdej kolbie była próbka innego metalu. Na te metale podziałano kwasem solnym. Opisane doświadczenie zilustrowano poniższym schematem.
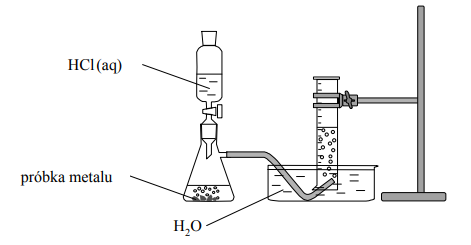
Podczas opisanego doświadczenia w każdej kolbie metal uległ całkowitemu roztworzeniu
i powstały klarowne, bezbarwne roztwory chlorków badanych metali. Przebiegowi wszystkich
reakcji towarzyszyło wydzielanie się bezbarwnego gazu.
Spośród czynności, których nazwy podano poniżej, wybierz tę, którą należy wykonać jako pierwszą w celu wyodrębnienia z każdej mieszaniny poreakcyjnej (powstałej podczas opisanego doświadczenia) jonowego produktu reakcji. Podkreśl jej nazwę.
Napisz w formie jonowej skróconej równanie reakcji glinu z kwasem solnym.
……………………………………………………………………………………………………………………………………
Przeprowadzono doświadczenie, w którym do probówki I wlano kwas solnyo pH = 2, a do probówki II – wodny roztwór kwasu octowego (etanowego) o pH = 2.
Arkusz maturalny z chemii rozszerzonej maj 2019 nowa formuła
Przeprowadzono doświadczenie, w którym do probówki I wlano kwas solny
o pH = 2, a do probówki II – wodny roztwór kwasu octowego (etanowego) o pH = 2. Roztwory miały temperaturę 298 K. Następnie do obu probówek dodano po 1 gramie pyłu cynkowego.
Opisane doświadczenie zilustrowano poniższym schematem.

Oceń, czy podane poniżej informacje są prawdziwe. Zaznacz P, jeśli informacja jest prawdziwa, albo F – jeśli jest fałszywa.