kwasy dikarboksylowe występujące w przyrodzie
Arkusz z chemii rozszerzonej czerwiec 2024 stara formuła
Poniżej przedstawiono wzory dwóch kwasów dikarboksylowych występujących w przyrodzie.

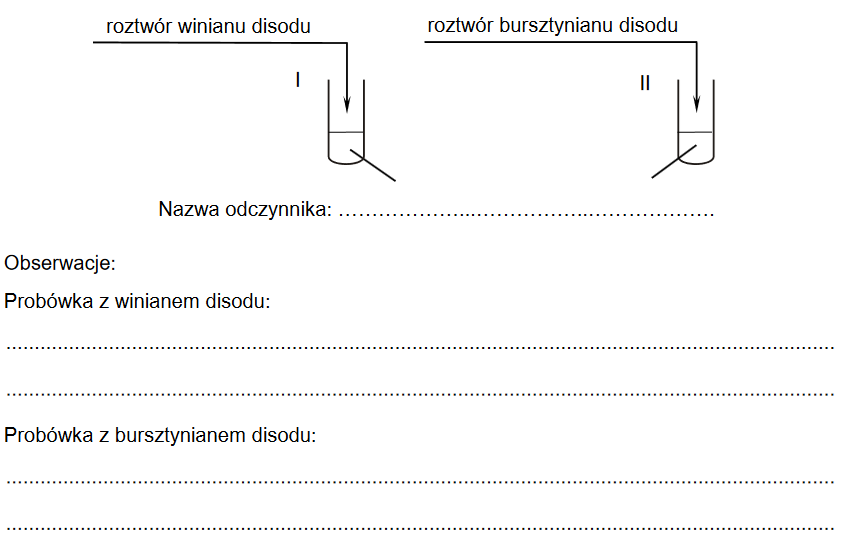
1. Przygotowano wodne roztwory soli sodowych kwasów: winowego i bursztynowego.
Uzupełnij schemat doświadczenia, które umożliwi rozróżnienie tych roztworów. Napisz nazwę odczynnika. Opisz obserwacje, które umożliwią identyfikację zawartości każdej probówki.
Lista odczynników:
− rozcieńczony kwas solny z oranżem metylowym
− wodny roztwór wodorotlenku sodu z fenoloftaleiną
− zalkalizowana świeżo strącona zawiesina wodorotlenku miedzi(II)
− mieszanina stężonych kwasów: azotowego(V) i siarkowego(VI).
2. Napisz równanie reakcji kwasu winowego z alkoholem metylowym w obecności kwasu siarkowego(VI), w której powstaje produkt zawierający w cząsteczce sześć atomów węgla. Zastosuj wzory półstrukturalne (grupowe) związków organicznych.

właściwości Kwasu winowego
Arkusz z chemii rozszerzonej czerwiec 2024 stara formuła
Kwas winowy jest stałą, krystaliczną substancją, dobrze rozpuszczalną w wodzie. Wodorowinian potasu KHC4H4O6, zwany kamieniem winnym, jest solą trudno rozpuszczalną w wodzie. Roztwarza się w wodnym roztworze wodorotlenku potasu.
1. Oceń prawdziwość poniższych zdań. Zaznacz P, jeśli zdanie jest prawdziwe, albo F – jeśli jest fałszywe.

2. Napisz w formie jonowej równanie reakcji, która zachodzi podczas roztwarzania wodorowinianu potasu w wodnym roztworze wodorotlenku potasu. Zastosuj wzory
półstrukturalne (grupowe) związków organicznych.
ciąg przemian związków organicznych
Arkusz z chemii rozszerzonej maj 2024 Formuła 2015
Na poniższym schemacie przedstawiono ciąg przemian związków organicznych A, B i C:
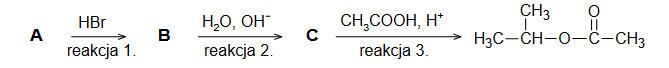
1. Napisz wzory półstrukturalne (grupowe) związków oznaczonych na schemacie literami A, B i C.
2. Określ typ reakcji (addycja, eliminacja, substytucja) oraz mechanizm (elektrofilowy, nukleofilowy, rodnikowy) reakcji oznaczonych na schemacie numerami 1. i 2.

wzory półstrukturalne fenyloalaniny
Arkusz z chemii rozszerzonej maj 2024 Formuła 2023
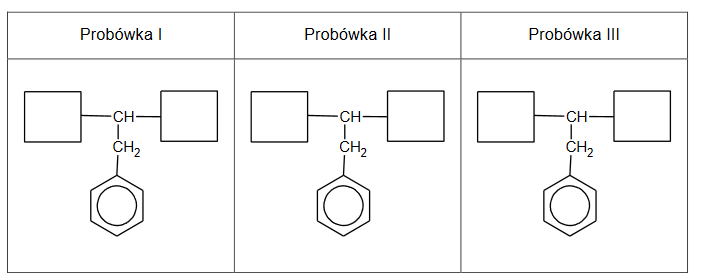
Przeprowadzono doświadczenie zilustrowane na poniższym rysunku:

Uzupełnij poniższe schematy, tak aby powstały wzory półstrukturalne (grupowe) fenyloalaniny w postaci, w której ten aminokwas będzie występował w dominującej formie w roztworze w każdej probówce.
Nomex – polimer stosowany do produkcji materiałów
Arkusz z chemii rozszerzonej czerwiec 2023 stara formuła
Nomex to polimer stosowany do produkcji materiałów o wysokiej odporności mechanicznej i termicznej. Fragment jego łańcucha przedstawiono poniżej:
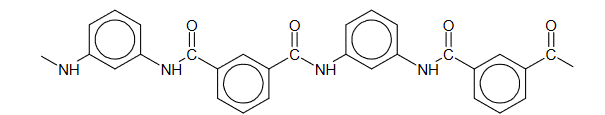
Monomery, z których można otrzymać nomex, różnią się charakterem kwasowo-zasadowym.
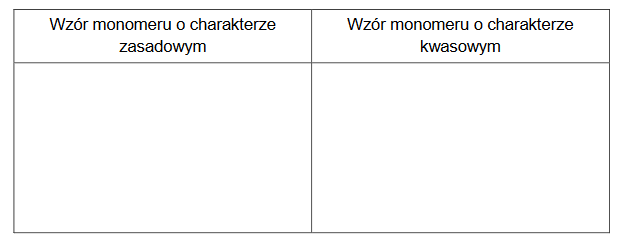
1. Uzupełnij tabelę. Narysuj wzory półstrukturalne (grupowe) lub uproszczone dwóch monomerów, z których można otrzymać ten polimer.
2. Uzupełnij zdania. Wybierz i podkreśl jedno określenie spośród podanych w każdym nawiasie.
Nomex otrzymuje się w wyniku polimeryzacji (łańcuchowej / kondensacyjnej). W tej przemianie (wydziela się / nie wydziela się) produkt uboczny.
otrzymywanie estrów w reakcjach alifatycznych
Arkusz z chemii rozszerzonej czerwiec 2023 nowa formuła
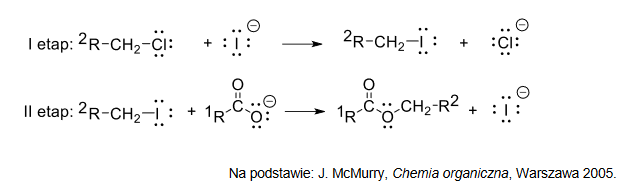
Estry można otrzymać w reakcji alifatycznych chlorowcopochodnych z solami kwasów karboksylowych. Poniżej przedstawiono mechanizm reakcji – zachodzącej w obecności jodków – między pierwszorzędowym halogenkiem alkilowym a anionem karboksylanowym:
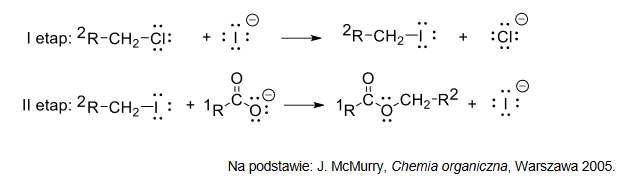
1. Napisz sumaryczne równanie reakcji anionu octanowego z 1-chlorobutanem. Zastosuj wzory półstrukturalne (grupowe) związków organicznych.
2. Uzupełnij poniższe zdania. Wybierz i zaznacz jedną odpowiedź spośród podanych w każdym nawiasie.
Opisane przemiany, w których udział biorą alifatyczne chlorowcopochodne i sole kwasów karboksylowych, są reakcjami (addycji / substytucji). Anion jodkowy pełni funkcję katalizatora i jego obecność skutkuje (obniżeniem / podwyższeniem) energii aktywacji oraz wzrostem (szybkości / wydajności) reakcji w porównaniu do reakcji prowadzonej bez jego udziału.