Reakcja aldolowa i jej produkt β-hydroksyaldehyd
Arkusz z chemii rozszerzonej marzec 2021
Reakcja aldolowa, przebiegająca w środowisku rozcieńczonej zasady, prowadzi do połączenia dwóch cząsteczek aldehydu lub ketonu i utworzenia wiązania między atomem węgla α jednej
cząsteczki i karbonylowym atomem węgla drugiej cząsteczki. Produktem jest β-hydroksyaldehyd (aldol) lub β-hydroksyketon. Reakcji ulegają wszystkie aldehydy i ketony zawierające atomy wodoru α, czyli atom wodoru zlokalizowany przy atomie węgla połączonym z grupą aldehydową lub ketonową. Jeśli etanal zostanie poddany działaniu zasady, takiej jak etanolan sodu lub wodorotlenek sodu, wówczas zachodzi szybka, odwracalna reakcja:
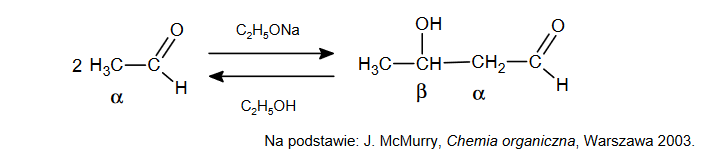
1. Napisz nazwę systematyczną produktu reakcji aldolowej etanalu.
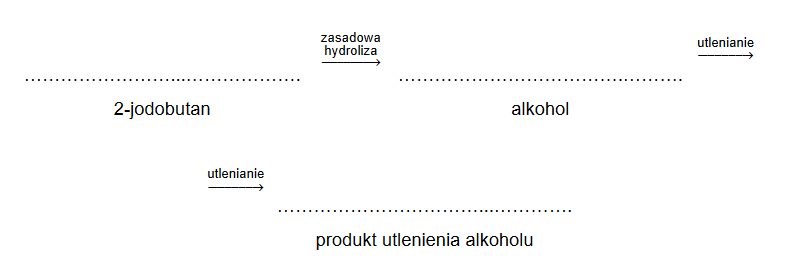
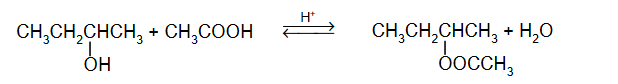
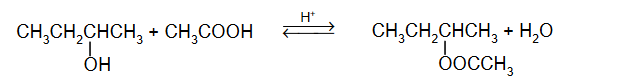
2. Napisz równanie reakcji aldolowej propanalu. Zastosuj wzory półstrukturalne (grupowe) związków organicznych.
właściwości redukujące kwasu metanowego
Arkusz z chemii rozszerzonej marzec 2021
Celem doświadczenia przedstawionego na poniższym schemacie było potwierdzenie właściwości redukujących kwasu metanowego.
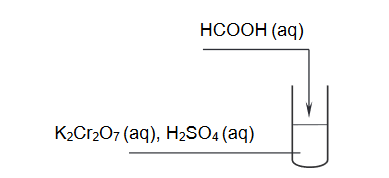
1. Spośród poniższych obserwacji wybierz i podkreśl wszystkie te zmiany, które można zaobserwować podczas wykonanego doświadczenia.
• wytrąca się zielony osad
• roztwór zmienia barwę z pomarańczowej na ciemnozieloną
• fioletowy roztwór się odbarwia
• roztwór zmienia barwę z pomarańczowej na żółtą
• wydziela się gaz
2. Wyjaśnij na podstawie budowy cząsteczki, dlaczego kwas metanowy wykazuje właściwości redukujące.
Rozpoznawanie związku po jego wzorze
Arkusz z chemii rozszerzonej marzec 2021
Poniżej przedstawiono wzór związku zawierającego azot.
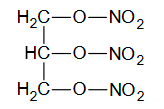
Zaznacz poprawne dokończenie zdania.
Związek o podanym wzorze jest
A. solą kwasu azotowego(III).
B. solą kwasu azotowego(V).
C. estrem kwasu azotowego(V).
D. związkiem nitrowym.
porównania mocy substancji chemicznych
Arkusz maturalny z chemii rozszerzonej lipiec 2020 Formuła 2015
W celu porównania mocy kwasu siarkowego(VI), fenolu, kwasu etanowego i kwasu węglowego przeprowadzono doświadczenie zilustrowane poniższym schematem. Wszystkie użyte roztwory zostały świeżo przygotowane.
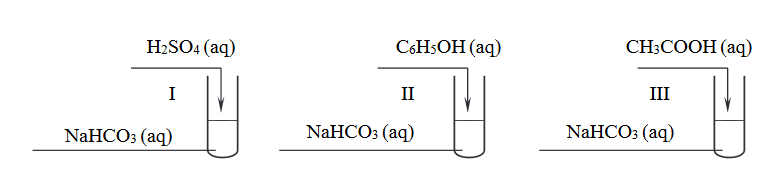
W probówkach I i III zaobserwowano wydzielanie się pęcherzyków gazu, a w probówce II – po zmieszaniu wodnych roztworów użytych do doświadczenia – nie przebiegła reakcja wodorowęglanu sodu z fenolem.
1. Sformułowane obserwacje i wnioski nie pozwalają na jednoznaczne określenie mocy badanych kwasów.
Jaką reakcję chemiczną należy dodatkowo przeprowadzić, aby możliwe było uszeregowanie wszystkich badanych kwasów od najsłabszego do najmocniejszego? Uzupełnij schemat – wybierz i podkreśl wzór jednego odczynnika z zestawu I oraz wzór jednego odczynnika z zestawu II.
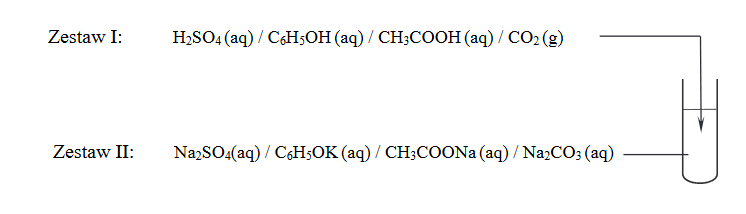
2. Napisz w formie cząsteczkowej równanie reakcji zachodzącej podczas dodatkowego doświadczenia.
identyfikacja pewnego estru
Arkusz maturalny z chemii rozszerzonej lipiec 2020 Formuła 2015
Ester E o masie molowej 178 g ∙ mol −1 zawiera 74,16% masowych węgla. Ten związek otrzymano w reakcji nasyconego monohydroksylowego alkoholu A wykazującego czynność
optyczną oraz monokarboksylowego aromatycznego kwasu B. Sól sodowa kwasu B jest stosowana jako konserwant.
1. Wykonaj odpowiednie obliczenia i ustal wzór półstrukturalny (grupowy) opisanego estru.
2. Napisz w formie jonowej skróconej równanie hydrolizy estru E przebiegającej w środowisku zasadowym.
kwas butanowy i jego monochloropochodne
Arkusz maturalny z chemii rozszerzonej kwiecień 2020 Formuła 2015
W poniższej tabeli zestawiono wartości stałej dysocjacji (w temperaturze 25 ºC) kwasu butanowego i jego monochloropochodnych.
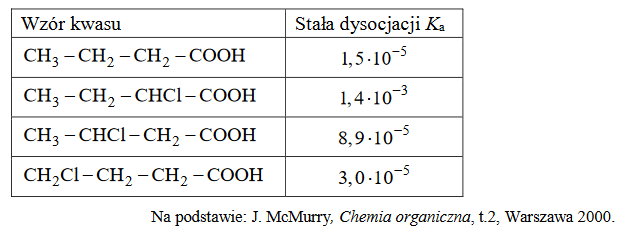
Oceń, czy poniższe informacje są prawdziwe. Zaznacz P, jeśli informacja jest prawdziwa, albo F – jeśli jest fałszywa.

reakcjz otrzymywania kwasów karboksylowych z aldehydów
Arkusz maturalny z chemii rozszerzonej kwiecień 2020 Formuła 2015
Reakcja utleniania propanalu odczynnikiem Tollensa przebiega zgodnie ze schematem:
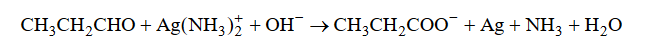
Napisz w formie jonowej z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo–elektronowy) równania procesów redukcji i utleniania
zachodzących podczas opisanej reakcji. Uwzględnij fakt, że reakcja zachodzi w środowisku zasadowym. Następnie uzupełnij schemat, tak aby otrzymać sumaryczne
równanie w formie jonowej skróconej opisanej reakcji utleniania propanalu.
Równanie procesu redukcji:
Równanie procesu utleniania:
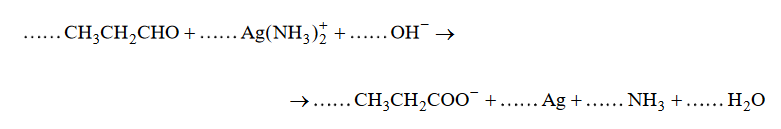
założenia teorii strukturalnej budowy związków organicznych
Arkusz maturalny z chemii rozszerzonej kwiecień 2020 Formuła 2015
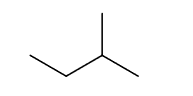
Wzory szkieletowe związków organicznych odzwierciedlają kształt łańcucha węglowego, dlatego lepiej oddają rzeczywistą strukturę cząsteczki. Są to wzory, w których nie zapisuje się symboli atomów węgla i połączonych z nimi atomów wodoru, ale rysuje się w postaci łamanej szkielet węglowy oraz zaznacza występujące w cząsteczce wiązania wielokrotne i zapisuje wzory grup funkcyjnych oraz symbole podstawników innych niż wodór, np. wzór szkieletowy
2-metylobutanu ma postać:
Poniżej przedstawiono wzory szkieletowe trzech związków organicznych.
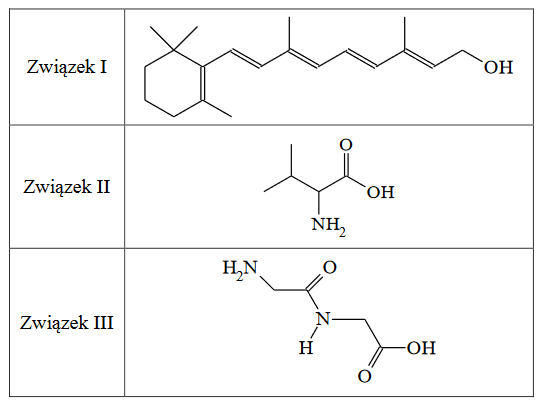
1. Napisz wzór sumaryczny związku II o wzorze szkieletowym podanym w tabeli.
2. Oceń, czy poniższe informacje są prawdziwe. Zaznacz P, jeśli informacja jest prawdziwa, albo F – jeśli jest fałszywa.

pyretryna – naturalna substancja owadobójcza
Arkusz maturalny z chemii rozszerzonej kwiecień 2020 Formuła 2015
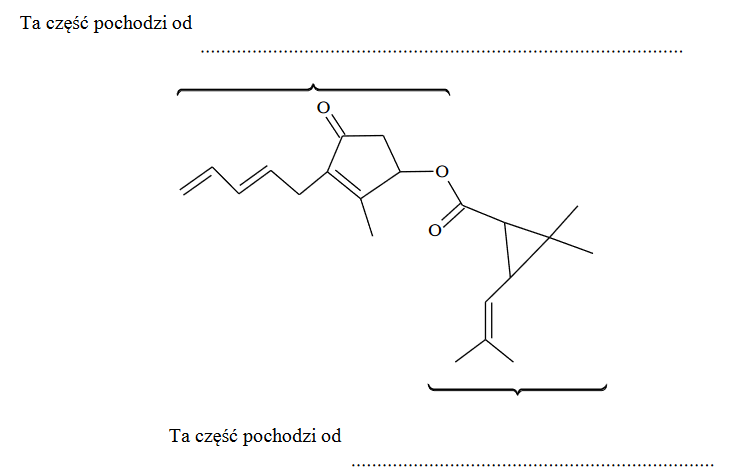
Poniżej przedstawiono wzór szkieletowy pyretryny, która jest naturalną substancją owadobójczą wyodrębnianą z pewnej odmiany chryzantem. Ten związek jest estrem.
W poniższym wzorze szkieletowym pyretryny zakreśl fragment stanowiący wiązanie estrowe oraz podpisz część pochodzącą od kwasu i część pochodzącą od alkoholu
porównanie budowy cząsteczek i właściwości skrobi i celulozy
Arkusz maturalny z chemii rozszerzonej kwiecień 2020 Formuła 2015
Poniżej przedstawiono dwuczłonowy fragment łańcucha celulozy.
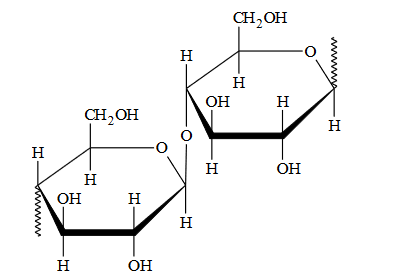
Celuloid jest tworzywem otrzymywanym przez reakcję celulozy z kwasem azotowym(V), w której wyniku estryfikacji ulegają dwie grupy hydroksylowe każdej jednostki glukozowej: połączone z drugim i szóstym atomem węgla jednostki glukozowej.
Uzupełnij poniższy schemat, tak aby otrzymać wzór jednoczłonowego fragmentu łańcucha opisanego diazotanu(V) celulozy.