Kwas etanodiowy o wzorze (COOH)2 jest najprostszym kwasem dikarboksylowym.
Arkusz maturalny z chemii rozszerzonej 2018 nowa formuła
Kwas etanodiowy o wzorze (COOH)2 jest najprostszym kwasem dikarboksylowym, którego
rozpuszczalność w wodzie w temperaturze 20 oC jest równa 9,52 g bezwodnego kwasu
w 100 g wody.
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2003.

Oblicz minimalną masę wody potrzebną do rozpuszczenia 14,0 gramów hydratu kwasu
etanodiowego o wzorze (COOH)2 · 2H2O w temperaturze 20 oC. Wynik końcowy podaj
w gramach i zaokrąglij do jedności.
Rozpoznawanie grup funkcyjnych w związakch organicznych.
Arkusz maturalny z chemii rozszerzonej 2018 nowa formuła
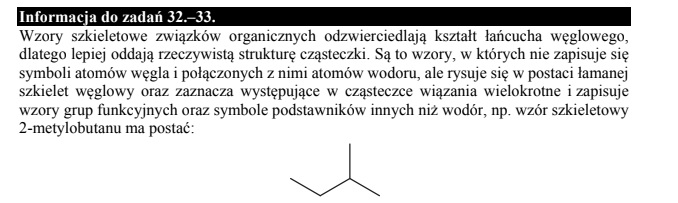
Poniżej przedstawiono wzory szkieletowe trzech związków organicznych.
Napisz wzór sumaryczny związku II o wzorze szkieletowym podanym w tabeli.
Oceń, czy poniższe informacje są prawdziwe. Zaznacz P, jeśli informacja jest prawdziwa,albo F – jeśli jest fałszywa.

Wzory szkieletowe związków organicznych.
Arkusz maturalny z chemii rozszerzonej 2018 nowa formuła

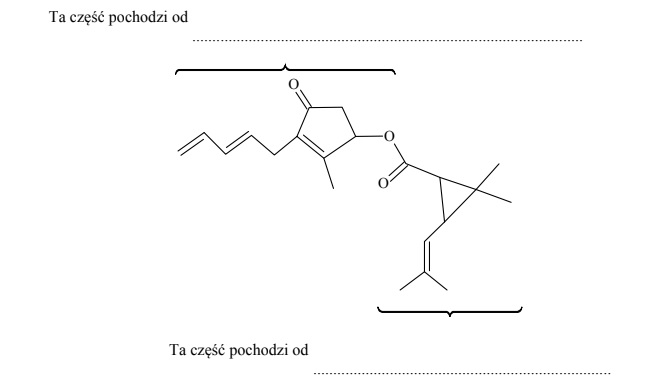
Poniżej przedstawiono wzór szkieletowy pyretryny, która jest naturalną substancją
owadobójczą wyodrębnianą z pewnej odmiany chryzantem. Ten związek jest estrem.
W poniższym wzorze szkieletowym pyretryny zakreśl fragment stanowiący wiązanie
estrowe oraz podpisz część pochodzącą od kwasu i część pochodzącą od alkoholu.
Przemiany węglowodorów.
Arkusz maturalny z chemii rozszerzonej 2018 maj stara formuła
Poniżej przedstawiono ciąg przemian chemicznych:
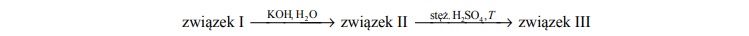
O związkach organicznych I, II i III wiadomo, że:
• związek I jest monobromopochodną alkanu
• związek II jest alkoholem trzeciorzędowym
• w cząsteczce związku III są cztery atomy węgla i osiem atomów wodoru.
Zidentyfikuj związki I, II i III i napisz ich wzory półstrukturalne (grupowe).

Równanie reakcji katalitycznego uwodornienia nitrobenzenu…
Arkusz maturalny z chemii rozszerzonej 2018 maj stara formuła
Poniżej przedstawiono ciągi przemian, w wyniku których otrzymano anilinę oraz etanol.
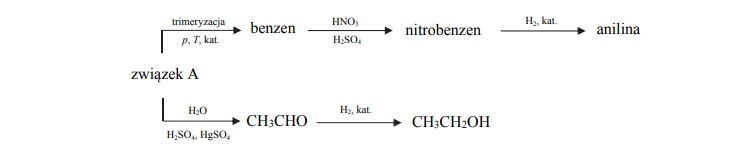
Napisz, stosując wzory półstrukturalne (grupowe) lub uproszczone wzory związków
organicznych, równanie reakcji katalitycznego uwodornienia nitrobenzenu oraz
równanie reakcji, w wyniku której ze związku A powstaje aldehyd
Równanie reakcji katalitycznego uwodornienia nitrobenzenu:
Równanie reakcji, w wyniku której ze związku A powstaje aldehyd:
Wpływ podstawnika na aktywność pierścienia aromatycznego. Nitrobenzen.
Arkusz maturalny z chemii rozszerzonej 2018 maj stara formuła
Podstawnik już obecny w pierścieniu aromatycznym wywiera wpływ na miejsce wprowadzenia
do niego kolejnego podstawnika w reakcjach elektrofilowych. Grupy alkilowe, –Cl, –Br, –NH2,
–OH kierują kolejny podstawnik w pozycje orto- i para- w stosunku do własnego położenia.
Obecność w pierścieniu aromatycznym grupy –NO2, –COOH czy –CHO powoduje, że kolejny
podstawnik jest wprowadzany głównie w pozycję meta-.
Na lekcji chemii uczniowie projektowali ciąg przemian chemicznych opisany poniższym
schematem.

Uczeń I zaproponował, aby najpierw przeprowadzić reakcję benzenu z chlorem (stosunek
molowy reagentów 1 : 1) w obecności FeCl3 jako katalizatora, a następnie na otrzymany
produkt podziałać mieszaniną nitrującą.
Uczeń II stwierdził, że należy najpierw przeprowadzić reakcję benzenu z mieszaniną nitrującą
i otrzymać mononitropochodną, a dopiero później na otrzymany produkt podziałać chlorem
(stosunek molowy reagentów 1 : 1) w obecności FeCl3 jako katalizatora.
Oceń projekty doświadczeń obu uczniów i wskaż ucznia (I albo II), który błędnie
zaprojektował doświadczenie. Uzasadnij swoje stanowisko.
Błędnie zaprojektował doświadczenie uczeń
Uzasadnienie:
Polimery PGA i PLA.
Arkusz maturalny z chemii rozszerzonej czerwiec 2017 stara formuła
Poniżej przedstawiono wzory PGA i PLA, popularnych polimerów, które w pełni ulegają biodegradacji.
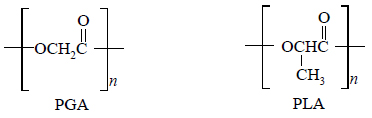
1. Podaj nazwę klasy tworzyw sztucznych, do których zakwalifikujesz PGA i PLA.
2. Podaj wzór półstrukturalny (grupowy) monomeru PGA i nazwę monomeru PLA.
Synteza propanonu.
Arkusz maturalny z chemii rozszerzonej czerwiec 2017 nowa formuła
Propanon można otrzymać z propenu na drodze dwuetapowej syntezy. Przebieg procesu zilustrowano na poniższym schemacie.
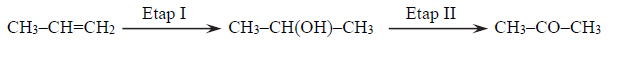
1. Spośród odczynników wymienionych poniżej wybierz te, które zastosowano w etapie I i etapie II opisanej syntezy, i wpisz ich wzory do tabeli.
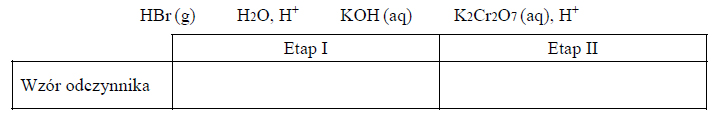
2. Określ typ (addycja, eliminacja, substytucja) i mechanizm (elektrofilowy, nukleofilowy, rodnikowy) reakcji, która zachodzi w etapie I, oraz napisz nazwę systematyczną organicznego produktu tego etapu.
3. Reakcja, która zachodzi w etapie II opisanej syntezy, jest reakcją utleniania i redukcji.
Oceń, czy związek o wzorze CH3–CH(OH)–CH3 jest w etapie II utleniaczem, czy – reduktorem, oraz określ liczbę moli elektronów, którą w tym etapie wymienia 1 mol tego związku.
Reakcja octanu sodu z zasadą sodową.
Arkusz maturalny z chemii rozszerzonej czerwiec 2017 nowa formuła
Sole sodowe kwasów karboksylowych w wyniku ogrzewania z wodorotlenkiem sodu ulegają dekarboksylacji (odszczepienie CO2) z utworzeniem węglowodoru.
Poniżej przedstawiono ciąg przemian chemicznych, w których biorą udział propanian sodu oraz związki organiczne umownie oznaczone literami Q, X, Y i Z.
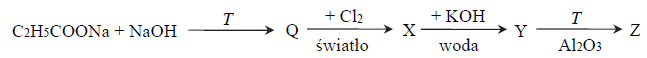
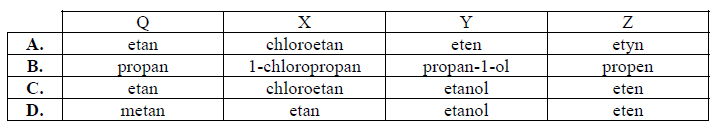
Zaznacz odpowiedź, w której podano poprawne nazwy związków Q, X, Y i Z.
Zadanie 19.
2017 maj SR
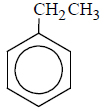
Napisz wzory uproszczone wszystkich pochodnych benzenu, które są izomerami związku o wzorze:
Dlaczego alken B nie występuje w postaci izomerów geometrycznych cis–trans
Arkusz maturalny z chemii rozszerzonej maj 2017 stara formuła
Spośród izomerycznych alkenów o wzorze sumarycznym C6H12 tylko alkeny A i B utworzyły w reakcji z HCl (jako produkt główny) halogenek alkilowy o wzorze:
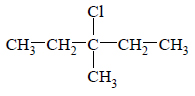
O tych alkenach wiadomo także, że alken A występuje w postaci izomerów geometrycznych cis–trans, a alken B – nie.
Napisz wzory półstrukturalne (grupowe) alkenów A i B. Wyjaśnij, dlaczego alken B nie występuje w postaci izomerów geometrycznych cis–trans.
Hydroliza halogenków alkilowych.
Arkusz maturalny z chemii rozszerzonej maj 2017 stara formuła
Halogenki alkilów ulegają zasadowej hydrolizie.
1. Napisz w formie jonowej, stosując wzory półstrukturalne (grupowe) związków organicznych, równanie hydrolizy zasadowej 2-bromo-2-metylopropanu. Napisz nazwę systematyczną organicznego produktu tej reakcji.
2. Określ mechanizm (elektrofilowy, nukleofilowy, rodnikowy) opisanej reakcji.
Etapy halogenwania alkanów.
Arkusz maturalny z chemii rozszerzonej maj 2017 nowa formuła
Poniżej podano ciąg przemian chemicznych:
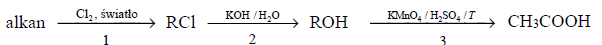
gdzie R – grupa alkilowa.
Halogenowanie alkanów (przemiana oznaczona na schemacie numerem 1) w obecności światła przebiega przez następujące etapy:
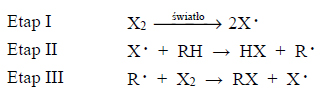
Szybkość tworzenia się halogenku alkilu zależy od szybkości, z jaką powstaje rodnik alkilowy.
Podkreśl numer najwolniejszego etapu reakcji oznaczonej na schemacie numerem 1.
Etap I, Etap II, Etap III