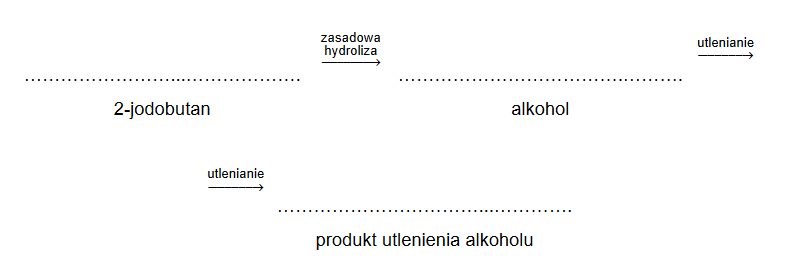
otrzymywanie alkenów poprzez reakcję eliminacji wody z alkoholi
Arkusz z chemii rozszerzonej maj 2021
Alkeny można otrzymać m.in. w wyniku reakcji eliminacji wody z alkoholi (tzw. reakcja dehydratacji alkoholi). Poddano dehydratacji 3-metylobutan-2-ol i otrzymano mieszaninę alkenów A i B, przy czym alken A jest produktem głównym (atom wodoru jest odrywany w tym przypadku od tego atomu węgla, który jest połączony z mniejszą liczbą atomów wodoru), a alken B – produktem ubocznym przemiany.
1. Produkt A można także otrzymać w wyniku dehydratacji innego alkoholu.
Podaj wzór półstrukturalny (grupowy) i nazwę systematyczną tego alkoholu.
Wzór:
Nazwa systematyczna:
2. Napisz równanie reakcji alkenu A z bromowodorem (HBr) prowadzącej do powstania produktu głównego tej przemiany. Zastosuj wzory półstrukturalne (grupowe) związków organicznych.
węglowodory pierścieniowe
Arkusz z chemii rozszerzonej maj 2021
Poniżej przedstawiono wzory dwóch związków organicznych: mentolu i tymolu.
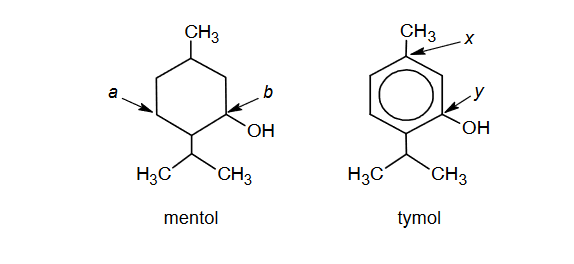
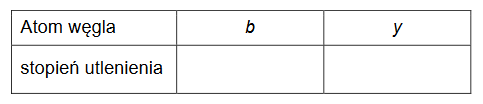
1. Uzupełnij poniższe tabele.
• Określ hybrydyzację orbitali walencyjnych: atomu węgla oznaczonego we wzorze mentolu literą a oraz atomu węgla oznaczonego we wzorze tymolu literą x.

• Określ formalne stopnie utlenienia: atomu węgla oznaczonego we wzorze mentolu literą b oraz atomu węgla oznaczonego we wzorze tymolu literą y.
2. Rozstrzygnij, czy cząsteczka tymolu jest chiralna. Odpowiedź uzasadnij.
Rozstrzygnięcie:
Uzasadnienie:
Kinetyka i statyka chemiczna
Arkusz z chemii rozszerzonej maj 2021
Do 500 cm³ wodnego roztworu kwasu metanowego (mrówkowego) o stężeniu 1 mol ∙ dm⁻³ dodano 500 cm³ wody. Temperatura otrzymanego roztworu nie uległa zmianie.
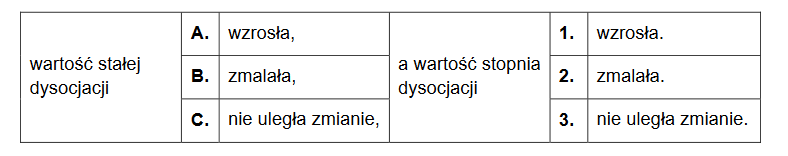
Dokończ zdanie. Zaznacz odpowiedź wybraną spośród A–C oraz odpowiedź wybraną spośród 1.–3.
Należy wnioskować, że po dodaniu wody do wodnego roztworu kwasu metanowego
cząsteczki kwasu etanowego tworzące dimer
Arkusz z chemii rozszerzonej maj 2021
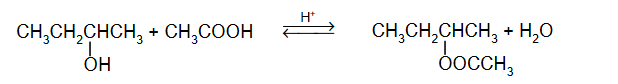
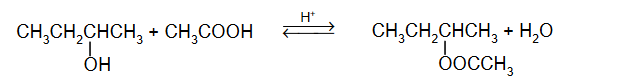
Cząsteczki kwasu etanowego mogą tworzyć dimer:
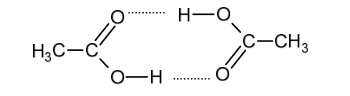
Dimer ten występuje w stanie gazowym oraz w roztworach kwasu etanowego w rozpuszczalnikach nietworzących z nim wiązań wodorowych.
Uzupełnij poniższe zdania. Wybierz i podkreśl jedną odpowiedź spośród podanych w każdym nawiasie.
Przedstawiony w informacji dimer powstaje w wyniku tworzenia się wiązań (kowalencyjnych / jonowych / wodorowych) między cząsteczkami kwasu etanowego. Rozcieńczony roztwór
kwasu etanowego w wodzie (nie zawiera dimerów / zawiera dimery), ponieważ woda (nie tworzy wiązań wodorowych / tworzy wiązania wodorowe) z cząsteczkami kwasu etanowego.
kondensacja aminokwasów
Arkusz z chemii rozszerzonej maj 2021
W wyniku kondensacji z jednej cząsteczki cysteiny (Cys) i dwóch cząsteczek leucyny (Leu) mogą powstać różne tripeptydy.
Napisz wszystkie możliwe sekwencje aminokwasów w tripeptydach o budowie liniowej – zastosuj trzyliterowe kody aminokwasów.
Sekwencje aminokwasów w tripeptydach: