elektroda bromosrebrowa – przykład elektrody halogenosrebrowej
EGZAMIN MATURALNY Z CHEMII POZIOM ROZSZERZONY MARZEC 2022
Przykładem elektrody halogenosrebrowej jest elektroda bromosrebrowa, której działanie opisano równaniem:
AgBr (s) + e– ⇄ Ag (s) + Br– (aq)
Potencjał tej elektrody zależy od stężenia jonów bromkowych i w temperaturze 298 K wyraża się równaniem:
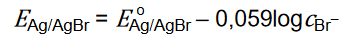
Standardowy potencjał tej elektrody EAg/AgBr = 0,071 V.
W temperaturze 298 K potencjał elektrody bromosrebrowej zanurzonej w wodnym roztworze bromku srebra pozostającym w równowadze z osadem tej soli był równy EAg/AgBr = 0,431 V.
Oblicz wartość iloczynu rozpuszczalności bromku srebra 𝑲𝒔[AgBr] w temperaturze 298 K.
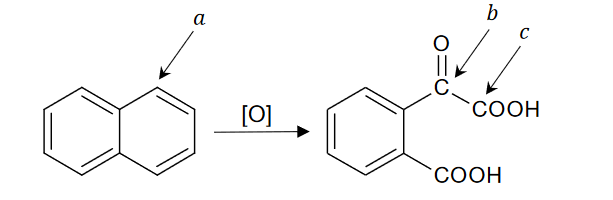
wzór półstrukturalny węglowodoru
EGZAMIN MATURALNY Z CHEMII POZIOM ROZSZERZONY MARZEC 2022
O dwóch węglowodorach A i B, z których każdy ma wzór sumaryczny C6H12, wiadomo, że:
• węglowodór A powstaje w wyniku reakcji między 3–bromo–2,2–dimetylobutanem
a alkoholowym roztworem wodorotlenku sodu przebiegającej w podwyższonej
temperaturze;
• węglowodór B, będący alkanem cyklicznym, powstaje w reakcji zachodzącej pomiędzy
dibromopochodną heksanu a cynkiem, a w jego cząsteczce obecny jest jeden
trzeciorzędowy atom węgla połączony m.in. z grupą metylową.
1. Napisz w formie jonowej skróconej równanie reakcji otrzymywania węglowodoru A. Zastosuj wzory półstrukturalne (grupowe) związków organicznych.
2. Narysuj wzór półstrukturalny (grupowy) lub uproszczony węglowodoru B oraz napisz jego nazwę systematyczną.

Nazwa systematyczna:
asymetryczne atomy węgla w estrach
EGZAMIN MATURALNY Z CHEMII POZIOM ROZSZERZONY MARZEC 2022
Poniżej przedstawiono wzór estru, w którego cząsteczkach są obecne dwa asymetryczne atomy węgla – oznaczone gwiazdką:
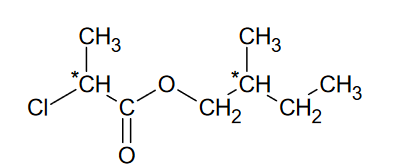
W laboratorium przeprowadzono reakcję, w której racemiczną mieszaninę kwasu 2–chloropropanowego (równomolową mieszaninę obu enancjomerów) poddano reakcji estryfikacji z jednym z enancjomerów 2–metylobutan–1–olu. W wyniku tej reakcji otrzymano dwa rodzaje estrów.
1.Rozstrzygnij, czy otrzymane estry są względem siebie enancjomerami. Uzasadnij odpowiedź.
Rozstrzygnięcie:
Uzasadnienie:
2. Napisz w formie jonowej skróconej równanie hydrolizy zasadowej estru opisanego w informacji. Zastosuj wzory półstrukturalne (grupowe) związków organicznych.
temperatury wrzenia amin
EGZAMIN MATURALNY Z CHEMII POZIOM ROZSZERZONY MARZEC 2022
Poniżej przedstawiono wzory trzech izomerycznych amin oznaczonych numerami I, II i III.
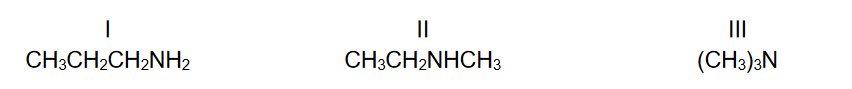
Wartości temperatury wrzenia tych amin, wymienione w przypadkowej kolejności, są równe: 3 °C, 36 °C, 47 °C.
Przyporządkuj aminom I–III wartości ich temperatury wrzenia.
I:
II:
III:
Wiązania peptydowe w białkach
EGZAMIN MATURALNY Z CHEMII POZIOM ROZSZERZONY MARZEC 2022
W wyniku hydrolizy 2,03 g pewnego peptydu o masie molowej równej 609,74 g * mol–1 otrzymano 2,27 g mieszaniny aminokwasów.
Oblicz, ile wiązań peptydowych zawiera cząsteczka badanego peptydu.
świeżo strącony wodorotlenek miedzi(II) z biuretem – efekty doświadczenia
EGZAMIN MATURALNY Z CHEMII POZIOM ROZSZERZONY MARZEC 2022
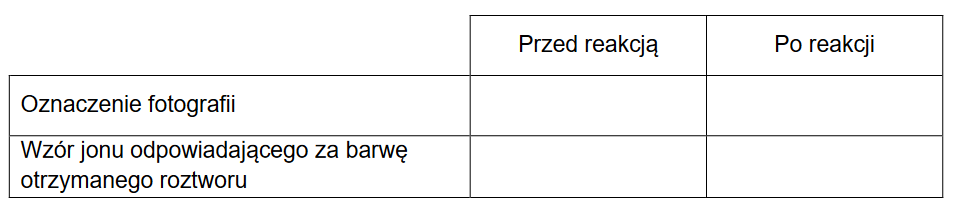
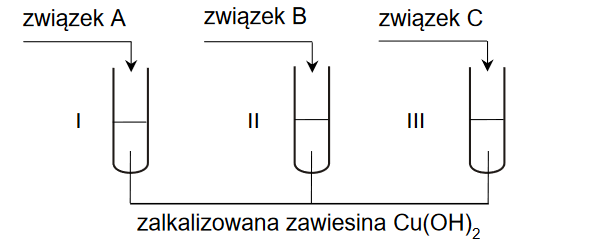
Przeprowadzono doświadczenie polegające na dodaniu świeżo strąconego wodorotlenku miedzi(II) do probówki zawierającej wodny roztwór biuretu H2N–CO–NH–CO–NH2.
Spośród poniższych ilustracji wybierz i zaznacz tę, która przedstawia efekt opisanego doświadczenia.

Kauczuk naturalny
EGZAMIN MATURALNY Z CHEMII POZIOM ROZSZERZONY MARZEC 2022
Poniżej przedstawiono wzór kauczuku naturalnego.
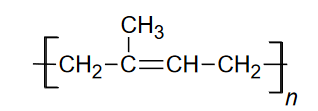
Dokończ zdanie. Zaznacz właściwą odpowiedź spośród podanych.
W laboratorium ten związek można otrzymać w reakcji polimeryzacji
A. 2–metylobut–1–enu.
B. 2–metylobuta–1,3–dienu.
C. 2–metylobut–2–enu.
D. 2–metylobuta–1,2–dienu.
D-alloza – izomer D-glukozy
EGZAMIN MATURALNY Z CHEMII POZIOM ROZSZERZONY MARZEC 2022
D–alloza to jeden z izomerów D–glukozy. W pewnych warunkach ten cukier może zostać utleniony do kwasu aldonowego lub kwasu aldarowego, co przedstawiono na poniższym
schemacie.
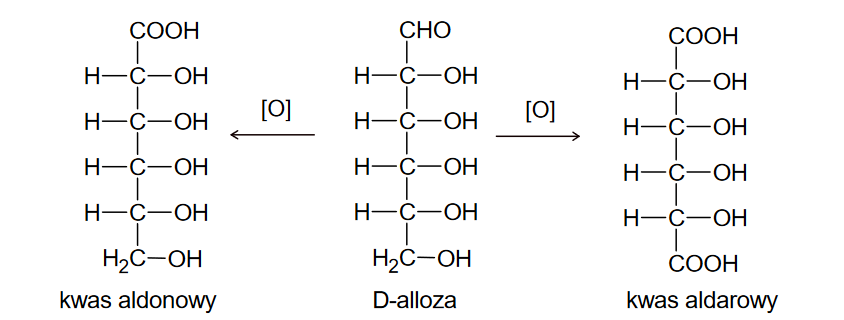
Oceń prawdziwość poniższych zdań. Zaznacz P, jeżeli zdanie jest prawdziwe, albo F – jeśli jest fałszywe.

Amigdalina – związek chemiczny występujący w gorzkich migdałach
EGZAMIN MATURALNY Z CHEMII POZIOM ROZSZERZONY MARZEC 2022
Amigdalina to związek chemiczny z grupy glikozydów, występujący w znacznych ilościach
w gorzkich migdałach. Wzór amigdaliny przedstawiono poniżej.
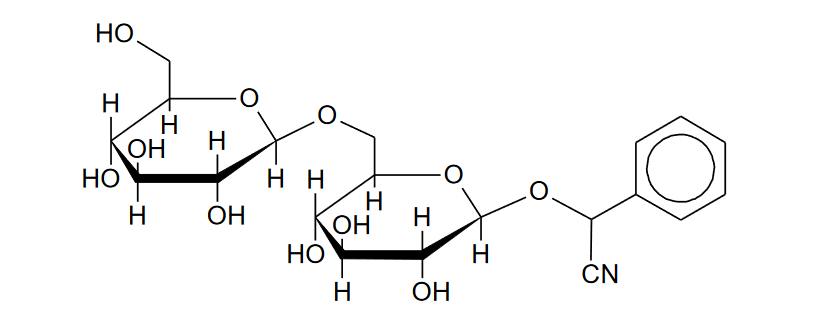
W wyniku hydrolizy amigdaliny zachodzącej w organizmie pod wpływem enzymów powstają trzy rodzaje drobin: cyjanowodór o wzorze HCN oraz dwa związki chemiczne, które w poniższym schemacie reakcji oznaczono literami A i B:
amigdalina + 2H2O → 2A + B + HCN
O związkach A i B wiadomo, że w odpowiednich warunkach ulegają reakcji z odczynnikiem Tollensa.
Napisz nazwę związku A oraz narysuj wzór związku B powstających w reakcji hydrolizy amigdaliny.
Nazwa związku A:
Wzór związku B: