hydroliza wodnego roztworu tetraoksokrzemianu(IV) sodu
Arkusz z chemii rozszerzonej czerwiec 2023 nowa formuła
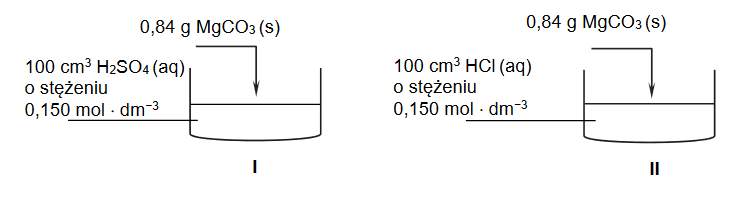
Stapianie tlenku krzemu(IV) z wodorotlenkiem sodu pozwala otrzymać różne krzemiany, w zależności od stosunku molowego substratów tej reakcji. Wskutek hydrolizy wodnego roztworu tetraoksokrzemianu(IV) sodu, czyli Na4SiO4, tworzy się roztwór silnie alkaliczny. Taki roztwór obok cząsteczek kwasu tetraoksokrzemowego(IV) zawiera wszystkie rodzaje wodoroanionów tego kwasu.
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2010
1. Napisz w formie cząsteczkowej równanie reakcji otrzymywania tetraoksokrzemianu(IV) sodu opisaną metodą. Oblicz stosunek masowy substratów.
Równanie reakcji:
Stosunek masowy:
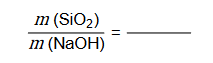
2. Napisz wzór sumaryczny tego wodoroanionu kwasu tetraoksokrzemowego(IV), który zbudowany jest z siedmiu atomów.
3. Narysuj elektronowy wzór kreskowy kwasu tetraoksokrzemowego(IV). Określ typ hybrydyzacji (sp, sp2, sp3) orbitali walencyjnych atomu krzemu w cząsteczce tego kwasu.
Elektronowy wzór kreskowy:
Typ hybrydyzacji:
zasady rozmieszczania elektronów na orbitalach
Arkusz diagnostyczny z chemii 2022 grudzień
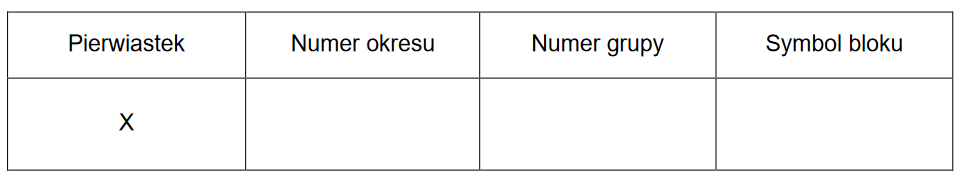
Na zdjęciu obok przedstawiono wodny roztwór soli, w skład której wchodzą pierwiastki X1, X2 i X3. Dwa z nich są w stanie wolnym metalami i należą do tego samego okresu, a jeden jest niemetalem i leży w innym okresie. Masy atomowe tych trzech pierwiastków, zaokrąglone do liczb całkowitych, spełniają zależność: M X1 + M X2 = M X3. Atom pierwiastka X3 ma na zewnętrznej powłoce dwa razy więcej elektronów niż atom pierwiastka X2, a atom pierwiastka X1 ma na zewnętrznej powłoce dwa razy więcej niesparowanych elektronów niż atom pierwiastka X2.

1. Zidentyfikuj pierwiastki X1, X2 oraz X3. Napisz ich symbole chemiczne.
X1:
X2:
X3:
2. Uzupełnij poniższą tabelę. Wpisz wartości liczb kwantowych odpowiadających niesparowanym elektronom w atomach (w stanie podstawowym) pierwiastków X1 i X3.

typowe właściwości chemiczne tlenków pierwiastków
Arkusz diagnostyczny z chemii 2022 grudzień
W trzech probówkach oznaczonych numerami 1, 2, 3, znajdowała się woda z dodatkiem oranżu metylowego. Do każdej z tych probówek wprowadzono małą porcję jednego z tlenków wybranych z poniższego zbioru:
Na₂O
SiO₂
P₄O₁₀
CuO
Zawartość każdej z probówek wymieszano i pozostawiono na pewien czas.

1. Uzupełnij tabelę. Wpisz wzory tlenków wprowadzonych do probówek 1 i 2.

2. Napisz w formie cząsteczkowej równanie reakcji, której produkt spowodował zmianę barwy oranżu metylowego w probówce 3.
Budowa atomu
EGZAMIN MATURALNY Z CHEMII POZIOM ROZSZERZONY MARZEC 2022
Na podstawie budowy atomów pierwiastków należących do grup 1.–2. oraz 13.–17. drugiego okresu układu okresowego uzupełnij poniższe zdanie. W wyznaczone miejsca wpisz symbol albo nazwę odpowiedniego pierwiastka.
Spośród pierwiastków drugiego okresu:
• najmniejszy ładunek jądra ma atom:
• najmniejszy promień atomowy ma atom:
• najmniejszą wartość pierwszej energii jonizacji ma atom:
świeżo strącony wodorotlenek miedzi(II) z biuretem – efekty doświadczenia
EGZAMIN MATURALNY Z CHEMII POZIOM ROZSZERZONY MARZEC 2022
Przeprowadzono doświadczenie polegające na dodaniu świeżo strąconego wodorotlenku miedzi(II) do probówki zawierającej wodny roztwór biuretu H2N–CO–NH–CO–NH2.
Spośród poniższych ilustracji wybierz i zaznacz tę, która przedstawia efekt opisanego doświadczenia.

porównanie aktywności chemicznej metali
Arkusz z chemii rozszerzonej czerwiec 2021
Przeprowadzono doświadczenie zgodnie z poniższym schematem.
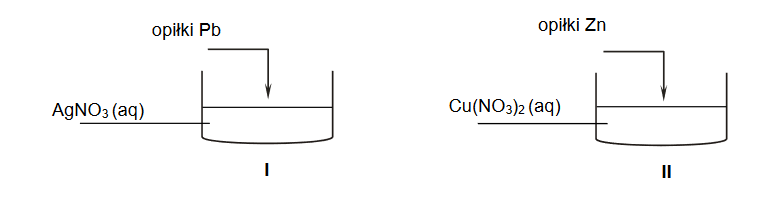
1. Napisz w formie jonowej skróconej równanie reakcji zachodzącej po dodaniu opiłków ołowiu do zlewki I. Rozstrzygnij, czy po zakończeniu doświadczenia masa roztworu w zlewce I wzrosła czy zmalała. Odpowiedź uzasadnij.
Równanie zachodzącej reakcji:
Rozstrzygnięcie:
Uzasadnienie:
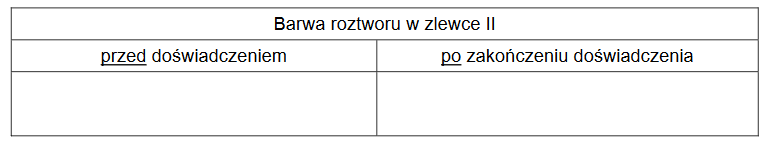
2. Po zakończeniu doświadczenia na dnie zlewki II znajdowały się dwa metale: cynk oraz miedź. Uzupełnij poniższą tabelę. Napisz, jaką barwę miał roztwór w probówce II przed reakcją i po jej zakończeniu.
reakcje zachodzące w roztworach wodnych
Arkusz z chemii rozszerzonej maj 2021
Przeprowadzono ciąg przemian chemicznych przedstawiony na poniższym schemacie.
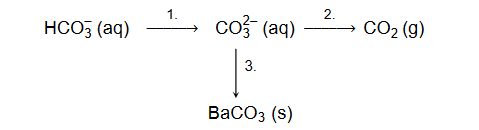
1. Spośród wymienionych odczynników
● wodorotlenek potasu
● kwas etanowy
● siarczan(VI) baru
● azotan(V) baru
wybierz i wpisz do tabeli nazwy lub wzory tych substancji, które mogły być użyte w poszczególnych etapach opisanego schematem ciągu przemian.
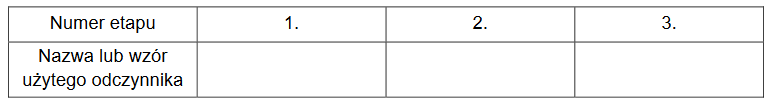
2. Napisz w formie jonowej skróconej równania reakcji oznaczonych na schemacie numerami 1. i 2.
Równanie reakcji 1.:
Równanie reakcji 2.:
planowanie i opisywanie doświadczeń
Arkusz z chemii rozszerzonej maj 2021
W dwóch probówkach znajdowały się wodne roztwory soli X i Z, otrzymane przez rozpuszczenie stałych soli, z których jedną był siarczek potasu, a drugą – bromek potasu. Przeprowadzono doświadczenie zgodnie z poniższym schematem. W doświadczeniu użyto świeżo otrzymanej wody chlorowej.
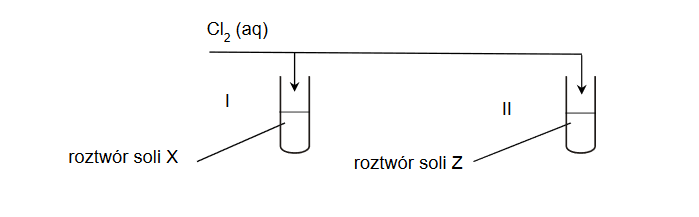
Po dodaniu wody chlorowej do probówek zauważono, że w probówce I roztwór zmienił barwę,
ale pozostał klarowny, natomiast w probówce II pojawiło się zmętnienie.
1. Zidentyfikuj sole X i Z i wpisz ich wzory do tabeli.
2. Napisz w formie jonowej skróconej równania reakcji pomiędzy chlorem a bromkiem potasu oraz pomiędzy chlorem a siarczkiem potasu.
właściwości chemiczne metali wobec rozcieńczonych i stężonych roztworów kwasów
Arkusz z chemii rozszerzonej maj 2021
W dwóch nieoznaczonych probówkach znajdowały się oddzielnie: rozcieńczony wodny roztwór kwasu azotowego(V) i rozcieńczony wodny roztwór kwasu siarkowego(VI). W tych roztworach zanurzono blaszki miedziane, a zawartość probówek lekko ogrzano.
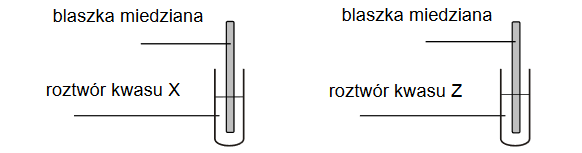
Po zanurzeniu blaszki miedzianej w roztworze kwasu X i ogrzaniu zawartości probówki wydzielał się bezbarwny gaz, który w kontakcie z powietrzem zabarwiał się na kolor czerwonobrunatny.
Uzupełnij poniższe zdania. Wybierz i podkreśl jedną odpowiedź spośród podanych w każdym nawiasie.
W rozcieńczonym roztworze kwasu azotowego(V) miedź (reaguje z wydzieleniem gazowego tlenku / reaguje z wydzieleniem wodoru / nie reaguje) i roztwór (przyjmuje barwę
niebieską / pozostaje bezbarwny). W rozcieńczonym roztworze kwasu siarkowego(VI) miedź (reaguje z wydzieleniem gazowego tlenku / reaguje z wydzieleniem wodoru / nie reaguje)
i roztwór (przyjmuje barwę niebieską / pozostaje bezbarwny). Kwasem X jest (HNO3 / H2 SO4).
analiza i porównanie właściwości chemicznych metali
Arkusz z chemii rozszerzonej marzec 2021
Do dwóch zlewek zawierających jednakowe objętości wody o temperaturze t = 20 °C dodano:
• do zlewki I – próbkę metalicznego magnezu
• do zlewki II – próbkę metalicznego wapnia.
Tylko w jednej zlewce zaobserwowano objawy reakcji chemicznej.
Napisz w formie jonowej równanie reakcji zachodzącej podczas opisanego doświadczenia. Wyjaśnij przyczynę różnej aktywności chemicznej badanych metali.
Równanie reakcji:
Wyjaśnienie: